HÒa tan hết 2.8g Fe cần dùng 400ml HCl thu được dung dịch X và V lít ở đktc
a. Tính nồng độ mol HCl cần dùng
b. Tính nồng độ của muối thu được trong dung dịch
Hòa tan hoàn toàn 11g hỗn hợp Fe và Al cần dùng 400ml dung dịch HCl. Sau phản ứng thu được 8,96 lít khí H2 thoát ra ở điều kiện tiêu chuẩn a) % khối lượng hỗn hợp kim loại ban đầu b) nồng độ mol dd HCl đã dùng c)nồng độ mol các muối sinh ra
a)
Gọi $n_{Fe} = a(mol) ; n_{Al} =b (mol) \Rightarrow 56a + 27b = 11(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
Theo PTHH : $n_{H_2} = a + 1,5b = \dfrac{8,96}{22,4} = 0,4(2)$
Từ (1)(2) suy ra : a = 0,1 ; b = 0,2
$\%m_{Fe} = \dfrac{0,1.56}{11}.100\% = 50,9\%$
$\%m_{Al} = 100\% - 50,9\% = 49,1\%$
b) $n_{HCl} = 2n_{H_2} = 0,8(mol)$
$\Rightarrow C_{M_{HCl}} = \dfrac{0,8}{0,4} = 2M$
c)
$C_{M_{FeCl_2}} = \dfrac{0,1}{0,4} = 0,25M$
$C_{M_{AlCl_3}} =\dfrac{0,2}{0,4} = 0,5M$
Hòa tan hoàn toàn 11,2g Fe vào dung dịch HCl 14,6% vừa đủ
a. Tính khối lượng dung dịch HCl cần dùng
b. Tính thể tích khí thu được ( đktc)
c, Tính nồng độ phần trăm của chất tan có trong dung dịch thu được
\(a,n_{Fe}=\dfrac{11,2}{56}=0,2(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{HCl}=0,4(mol)\\ \Rightarrow m_{dd_{HCl}}=\dfrac{0,4.36,5}{14,6\%}=100(g)\\ b,n_{H_2}=0,2(mol)\\ \Rightarrow V_{H_2}=0,2.22,4=4,48(l)\\ c,n_{FeCl_2}=0,2(mol)\\ \Rightarrow C\%_{FeCl_2}=\dfrac{0,2.127}{11,2+100-0,2.2}.100\%\approx 22,93\%\)
Câu 44: Hòa tan hoàn toàn 2,8 gam Fe cần dùng vừa đủ dung dịch axit HCl 7,3% thu được dung dịch muối X và thấy thoát ra V lít khí H2 (ở đktc)
a. Tính giá trị của V?
c. Tính khối lượng dung dịch axit HCl đã phản ứng?
c. Tính nồng độ phần trăm của muối trong X?
d. Lượng Hiđro thu được ở trên cho tác dụng 16 gam oxit của kim loại R(II). Xác định tên kim loại R?
Cho 12,48 gam X gồm Cu và Fe tác dụng hết với 0,15 mol hỗn hợp khí gồm Cl2 và O2, thu được chất rắn Y gồm các muối và oxit. Hòa tan vừa hết Y cần dùng 360 ml dung dịch HCl 1M, thu được dung dịch Z. Cho dung dịch AgNO3 dư vào Z, thu được 75,36 gam chất rắn. Mặt khác, hòa tan hết 12,48 gam X trong dung dịch HNO3 nồng độ 31,5%, thu được dung dịch T và 3,36 lít khí NO (sản phẩm khử duy nhất, ở đktc). Nồng độ % của Fe(NO3)3 trong T gần nhất với giá trị nào sau đây?
A. 7,28.
B. 5,67.
C. 6,24.
D. 8,56.
Chọn B
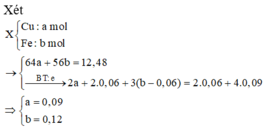
Khi cho X tác dụng với HNO3 thu được dung dịch T gồm Fe(NO3)2 (x); Fe(NO3)3 (y); Cu(NO3)2 (0,09).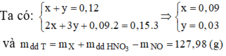
Vậy C% Fe(NO3)3 = 5,67%
Cho 12,48 gam X gồm Cu và Fe tác dụng hết với 0,15 mol hỗn hợp khí gồm Cl2 và O2, thu được chất rắn Y gồm các muối và oxit. Hòa tan vừa hết Y cần dùng 360 ml dung dịch HCl 1M, thu được dung dịch Z. Cho dung dịch AgNO3 dư vào Z, thu được 75,36 gam chất rắn. Mặt khác, hòa tan hết 12,48 gam X trong dung dịch HNO3 nồng độ 31,5%, thu được dung dịch T và 3,36 lít khí NO (sản phẩm khử duy nhất, ở đktc). Nồng độ % của Fe(NO3)3 trong T gần nhất với giá trị nào sau đây?
A. 7,28
B. 5,67
C. 6,24
D. 8,56
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch axit HCl 7,3% thu được dung dịch muối X và thấy thoát ra V lít khí H2 (ở đktc) a. Tính giá trị của V? b. Tính khối lượng dung dịch axit HCl đã phản ứng? c. Tính nồng độ phần trăm của muối trong X?
a)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2-->0,4----->0,2--->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
b) mHCl = 0,4.36,5 = 14,6 (g)
=> \(m_{dd.HCl}=\dfrac{14,6.100}{7,3}=200\left(g\right)\)
c)
mdd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
mZnCl2 = 0,2.136 = 27,2 (g)
=> \(C\%=\dfrac{27,2}{212,6}.100\%=12,8\%\)
Ngâm 8,4g Fe trong dung dịch 100ml CuSO4 1M, cho đến khi phản ứng kết thúc thu được chất rắn A và dung dịch B. Hòa tan chất rắn A trong dung dịch HCl dư thoát ra V lít khí ở đktc
a) Tính V?
b)Tính nồng độ mol của dung dịch B.Biết rằng thể tích dung dịch thay đổi không đáng kể.
\(n_{CuSO_4}=0,1.1=0,1\left(mol\right)\)
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
PTHH: Fe + CuSO4 --> FeSO4 + Cu
Xét tỉ lệ \(\dfrac{0,1}{1}< \dfrac{0,15}{1}\) => CuSO4 hết, Fe dư
PTHH: Fe + CuSO4 --> FeSO4 + Cu
_____0,1<---0,1---------->0,1
Fe + 2HCl --> FeCl2 + H2
0,05------------------->0,05
=> VH2 = 0,05.22,4 = 1,12(l)
b) \(C_{M\left(FeSO_4\right)}=\dfrac{0,1}{0,1}=1M\)
hoà tan hoàn toàn 20,4g hỗn hợp Cu,Fe trong 200ml dung dịch HCL sau phản ứng thu được 5,6 lít khí ĐKTC
a) tính khối lượng Fe đã phản ứng
b) tính nồng độ mol của dung dịch HCL
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH :
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,25 0,5 0,25
\(a,m_{Fe}=0,25.56=14\left(g\right)\)
\(b,C_{M\left(HCl\right)}=\dfrac{0,5}{0,2}=2,5\left(M\right)\)
Câu 1: Hòa tan hoàn toàn 16 gam đồng (II) oxit CuO cần dùng 300 gam dung dịch HCl thu được dung dịch X.
a) Tính khối lượng muối thu được trong dung dịch X.
b) Tính nồng độ phần trăm dung dịch HCl phản ứng.
c) Tính nồng độ phần trăm của muối trong dung dịch X.
giải dùm với ạ , đang cần gấp ạ
Ta có: \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PT: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
______0,2_____0,4_____0,2 (mol)
a, \(m_{CuCl_2}=0,2.135=27\left(g\right)\)
b, \(m_{HCl}=0,4.36,5=14,6\left(g\right)\Rightarrow C\%_{HCl}=\dfrac{14,6}{300}.100\%\approx4,867\%\)
c, Ta có: m dd sau pư = 16 + 300 = 316 (g)
\(\Rightarrow C\%_{CuCl_2}=\dfrac{27}{316}.100\%\approx8,54\%\)